沈建飞医生的科普号
- 精选 原位腺癌和微浸润腺癌患者的长期预后
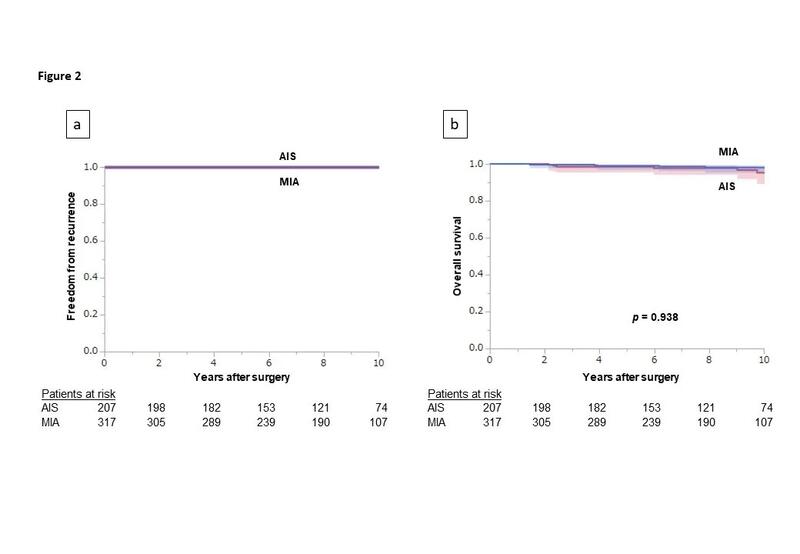
简介:WHO对肺肿瘤的分类将原位腺癌(AIS)和微浸润腺癌(MIA)定义为无组织浸润成分或组织浸润成分有限的癌症。AIS或MIA患者术后5年无复发的可能性已显示为100%。这项研究旨在分析术后5年以上的AIS或MIA患者的预后。 方法:我们回顾了1998年至2010年间4768例行肺癌切除术的患者的病理结果。其中,包括524例行AIS根治性切除术的患者(207例,占39.5%)和MIA(317例,60.5%)。此外,我们还分析了继发原发性肺癌的术后复发,生存率和发展情况。 结果:在纳入的患者中,女性为342例(65.3%),非吸烟者为333例(63.5%),肺叶切除术后为229例(43.7%)。平均病理总肿瘤直径为15.2±5.5mm。术后中位随访期为100个月(范围:1-237)。AIS或MIA病例均未观察到肺癌复发。估计AIS / MIA病例术后10年的疾病特异性生存率分别为100%/ 100%(p = 0.72),总生存率分别为95.3%/ 97.8%(p = 0.94)。术后10年异时性原发性肺癌的估计发病率分别为AIS 5.6%和MIA 7.7%(p = 0.45),且与EGFR突变状态无关。 结论:尽管应关注发展为异时性继发性肺癌的可能,但其在切除AIS和MIA后5年以上复发的风险非常低。这一发现增强了将AIS和MIA与其他肺腺癌区分开来的临床价值。 自2015年世界卫生组织(WHO)发布第四版肺肿瘤分类以来,就已经正式定义了原位腺癌(AIS)和微浸润性腺癌(MIA)。(BAC)肿瘤大小在3厘米或更小且没有任何侵袭,因此被重新命名为AIS。以前被归类为BAC混合腺癌且浸润不超过0.5 cm的肿瘤被重新命名为MIA。这些定义基于国际肺癌研究协会,美国胸科学会和欧洲呼吸学会认可的多学科小组的建议,目的是更好地了解疾病并改善患者护理。定义AIS和MIA的分类的概念是,由于AIS的组织学浸润前性质和MIA的侵入性成分有限,因此在完全切除肿瘤后,它们应具有100%或接近100%的无复发可能性。 确实,许多报告都描述了切除AIS或MIA后的良好无复发生存(RFS)状态。据我们所知,AIS或MIA手术后5年内未报告复发。但是,只有少数小型研究报告了长期(> 5年)结果。最近,美国国家肺部筛查试验显示,低剂量螺旋计算机断层扫描(CT)可以降低选定患者的肺癌死亡率。由于使用低剂量CT筛查的患病率不断上升, 包括AIS和MIA在内的分期肿瘤将被更频繁地发现。为了更好地管理AIS和MIA,评估这些类型肿瘤的手术后长期效果非常重要。在本研究中,我们旨在阐明完全切除后AIS和MIA的长期预后。 材料和方法 患者收集和组织学评估 在1998年至2010年间,在日本东京国立癌症中心医院接受手术切除的4,768例肺癌患者中,我们回顾性收集了3,170例肺腺癌患者的数据。 对于每个手术,从经支气管或经胸膜注射(处于充气状态)对切除的标本进行固定,依次切成5毫米厚的切片,并进行宏观福尔马林检查。接下来,从所选的组织块上切下连续的4 ?m厚切片,并根据需要用石蜡切片法,苏木精和曙红,Elastica-van Gieson以及高碘酸-席夫(Schiff)染色制备制备标本。 两名以上的病理学家根据世界卫生组织第四版《肺肿瘤分类》对所有适用于腺癌病例的幻灯片进行了组织病理学评估。因此,将腺癌的侵袭性成分定义为:1)除鳞状上皮以外的组织学亚型(即,乳头状,腺泡状,微乳头状和/或实体状);2)肿瘤细胞浸润肌成纤维细胞基质;3)淋巴,血管,胸膜和空域入侵;4)散布在空气空间中。AIS在组织学上被定义为小的(≤3 cm)局限性腺癌,其生长仅限于沿既有的肺泡结构的肿瘤细胞(纯粹的鳞状细胞生长),并且缺乏基质,血管或胸膜浸润。不存在腺泡,乳头状,实性或微乳头状等侵入性模式。MIA在组织学上被定义为小(≤3 cm)的孤立性腺癌,主要表现为在最大尺寸上呈血型且≤5 mm浸润。AIS和MIA的代表性组织学图如图1所示。在最大尺寸上测量了浸润的大小。当有多个病灶时,通过累加侵袭性成分的百分比并将其乘以总肿瘤直径来估计侵袭的大小。通过肉眼检查来测量肿瘤的总大小。如果肉眼检查和显微镜检查之间的大小有差异,则优先考虑显微镜检查的结果。 在排除了具有其他肺癌,同步浸润性肺癌或不完全切除的当前或先前治疗史的病例后,我们最终收集了524例,包括AIS(207例,39.5%)和MIA(317例,60.5%)。完全切除定义为所有宏观肿瘤组织的切除和显微分析后的切缘没有肿瘤细胞。在患有多个AIS或MIA的患者中,我们收集了MIA侵袭性成分最大或AIS肿瘤总直径最大的肿瘤数据。 所有临床信息均摘自患者的病历。收集患者的手术年龄,性别,吸烟习惯,肿瘤位置,手术步骤,肿瘤大小和亚叶切除术的边缘距离(如果有)。 EGFR突变评估 如果有标本,则使用高分辨率熔解分析检测到两个常见的表皮生长因子受体(EGFR)突变,即第19外显子的缺失(Ex19del)和第21外显子的密码子858的点突变(L858R)。 病人随访 我们记录了术后常规随访期间的肿瘤复发情况。随访评估包括身体检查,血液分析(包括癌胚抗原),胸部X线摄影以及胸部和腹部CT。每当患者出现提示复发的症状或体征时,都将使用脑磁共振成像,颈部,胸部和腹部的正电子发射断层扫描和/或骨闪烁显像进行进一步评估。根据这些评估结果诊断出肿瘤复发。随访一直进行到2020年3月。 放射学上,异时性继发性原发性肺癌(SPLC)的定义如下:所有结节的合并/肿瘤比(CTR)均大于0.5的多个新的肺结节被定义为初始原发性肺癌的复发性病变,而其他多个 新的肺部新结节被定义为SPLC。CTR是固体成分大小(合并)与肿瘤总直径之比。与先前手术切除的边缘分开发展的单个新结节被认为是SPLC。这些定义是基于日本临床肿瘤学小组(JCOG)进行的研究中使用的协议。 当对新的肺部病变进行组织学评估时,确定新病变是SPLC还是复发是基于两名以上病理学家对最初切除的肿瘤和新的肺部病变的比较。 统计分析 数据以均值,中位数或计数和百分比表示。为了对AIS / MIA与性别,肿瘤位置,手术程序,吸烟习惯和SPLC发生率之间的关系进行统计分析,使用了Pearson检验。视情况使用学生t检验或Mann-Whitney U检验比较AIS和MIA组中变量的平均值。使用Kaplan-Meier方法估算了总生存期(OS),肺癌特异性生存期(CSS)和无复发率以及SPLC的发生率,并使用 对数等级测试。所有测试均为双面测试,p值
 沈建飞 副主任医师 台州医院 心胸外科2897人已读
沈建飞 副主任医师 台州医院 心胸外科2897人已读 - 精选 2016 亚洲共识指南:肺结节的评估
2016-07-07 21:06来源:丁香园作者:沈建飞字体大小2016 年 2 月,亚洲肺部疾病和胸外科多学科专家小组在美国胸科医师学会(ACCP)制定的肺结节评估指南的基础上结合亚洲患者的自身特点制订了亚洲肺结节患者的评估指南。来自亚洲的多学科小组针对 ACCP 指南进行讨论,并认为在达成共识前,需要进一步调查。修订建议分发到每个小组成员,小组成员反复审查并重新起草最终指南。亚洲肺结节的评估与 APCC 指南中所指出的重要注意事项大致相同。但该指南指出临床医生应该重视室内和室外空气严重污染导致的肺癌风险,还有女性非吸烟人群肺腺癌的高发。此外,对于肉芽肿性疾病和其他感染性疾病在亚洲高发病率高也应引起注意。总体来说,应该考虑延长 ACCP 推荐的对肺结节的观察时间。亚洲由于肺结核高发,不宜对于肺部结节用 PET 进行筛查,应采用非手术活检确诊和定期监测。最后希望亚洲的医生应将该共识常规用于临床实践,以达到对肺结节的评估的一致性。简介肺结节主要是指肺实质内单发或多发直径不超过 3 cm 的圆形或类圆形结节影,不能排除早期肺癌的可能。因此,临床医生需要准确地描述肺结节,特别是那些有恶性可能的结节。临床医生可以根据结节性质制定合适的治疗计划,继续观察或明确诊断及治疗。根据定义,肺结节不伴有肺门及纵隔淋巴结肿大、肺不张或肺炎等其他疾病。美国胸科医师学会(ACCP)制定的肺结节评估指南已出版。尽管对这些指南的认识度很高,但是亚洲国家的临床医生对这些临床指南的实践率却很低。ACCP 建议,临床实践指南应该「入乡随俗」、「因地制宜」,这样才能更容易被实施。多学科专家小组致力于完善 ACCP 的推荐,使其成为适用于亚洲的临床指南。亚洲许多国家肺癌发生率高,尤其是在吸烟率高的国家。对于种族、遗传、患病风险,需要治疗的良性病变的发病率、恶性病变的发病率、获得诊断的机会还有对疾病的了解等,亚洲患者都有其独特性。亚洲肺结核发病率高,这意味着就算是良性的肺结节也需要得到明确的诊断,以保证个人和公共健康。在西欧,加拿大和美国等,肺结核的发病率小于 10/10 万人 / 年。相反,在亚洲,虽然在一些高收入的国家比它们发病率还低(例如日本),但大部分国家还是要比它们的发病率(10 万人 / 年,中国 70 例,印度 171 例,泰国 119 例)。在亚洲不同国家对肺结节的评价指南存在差异。中国,韩国及日本都有本国的指南,而新加坡、印度和泰国这些没有全国性指南的国家则按照它们当地机构的规范对肺结节进行评价。在一项亚洲地区内的非官方调查中发现,有一些经常在临床中的实践中与 ACCP 指南所建议的相饽。制定临床实践指南的目的是在 ACCP 肺结节评估指南的基础上,结合亚洲患者的特点制订适用于亚洲患者肺结节评估的指南。推荐肺结节初诊的主要目标是尽可能确诊,避免一些无需治疗的良性病变患者接受侵入性的检查。无论是良性还是恶性肺结节都能在 CT 上显实性或半实性影。对于实性结节,其良恶性的可能性受患者的年龄,吸烟史,结节大小,有无分叶、咯血、钙化,有无肿瘤史,肺结核史和其他肺部良性疾病史,还有 PET 的摄取率等因素的影响(表 1)。半实性结节分为非实性结节(磨玻璃结节)和部分实性结节(有实性成分,但磨玻璃成分≧50%)。表 1 CT 提示为恶性肿瘤的影像学特征参数恶性结节的特征生长速度倍增时间为20-400天(大多数的实性结节<100天);磨玻璃结节和半实性结节增长速度较慢(>200天);如果增长速度非常快提示是感染或炎症位置肺结节分布在两肺上叶恶性病变的可能性较大(亚洲因肺结核发病率较高导致其诊断的意义减低)边缘分叶状与恶性密切相关;凹陷征一般出现在明显的浸润的腺癌中空洞不规则厚壁空洞(壁厚> 15 mm)与恶性病变相关大小结节随着其最大直径的增大其恶性病变的可能性也逐渐增大(> 2 cm的结节为恶性的可能性较大,但﹤2 cm的结节也不能排除恶性病变的可能性)钙化结节内钙化为小斑点,靠近边缘时,为恶性病变的可能性大其他血管集束征、支气管充气征半实性结节可以是炎症,或者是各种的外周型腺癌,包括癌前病变非典型瘤样增生、原位癌和各种亚型的腺癌。半实性结节,特别是纯磨玻璃结节,一般生长缓慢,其恶性程度大小与结节大小相关,但与吸烟史关系不大。下列是亚洲专家小组根据 ACCP 指南修改制定的肺结节评估指南。对于指南的修改之处和额外补充的指南及其理由以下予以补充说明。1. 不确定性质的结节(图 1)在没有明确的诊断前,所有新发现的肺结节性质都是未定的。一些如弥散状、斑片状硬,爆米花状钙化影像学特征提示结节为良性病变。在亚洲很多国家都有常规的胸片体检,造成很多的肺结节被发现。尽管专家小组发现数字 X 射线成像的过渡使之前的 X 线胶片很难与数字图像作对比,但 ACCP 指南的这一推荐在亚洲仍适用。对比放射线影像可评估结节大小的变化。几乎没有证据支持对实性结节进行 2 年一次 CT 监测。但对于肺癌高危人群,需要根据国际指南和当地保健标准每年做低剂量螺旋 CT 筛查。与胸片相比,CT 能够了解结节的位置,形状,边缘和衰减等特征。专家小组强调,薄层 CT(≤ 1 mm)更能够了解结节的影像学特征。结节大小的测量可以帮助了解结节是否生长。图 1 不确定性质的结节处理流程2. > 8 mm 性质未明的实性结节(图 2)专家小组完善这一新推荐是为了适应亚洲国家临床实践条件和可供利用资源巨大变化。此外,专家小组建议由内科医生、外科医生、影像科医生和病理科医生共同制定患者的治疗方案。在亚洲的许多国家,最初的结节良恶性的评估用的是临床判断。临床医生希望通过定量模型来预测结节为恶性的可能性,但要注意,这些模型并未在亚洲人群中验证。事实上,可以通过目标人群,易用性,和验证的程度指导 ACCP 指南建议的定量模型的选择。个人的地域和文化环境可能对患者对于这个「小概率的可能性」的在意程度有所不同。总体来说,亚洲人群肺结节为恶性病变的可能性要比欧洲人群要高。看似良性的结节(为恶性的概率很低的结节)有时候准确的诊断要比监测更加必要。例如:肺结核或其他需要特殊治疗的感染性疾病还有大量使用免疫抑制剂的患者(如移植)需要采取积极的治疗。图 2 > 8 mm 性质未明的实性结节的处理流程在亚洲,肺癌的危险因素高发,有报道指出,大小稳定的结节在多年之后出现恶变,这暗示着根据临床的判断和病人的意愿每年监测的时间应该扩大(3 年或以上)。但专家小组发现缺乏支持这一做法的证据还有持续辐射带来的潜在风险。若结节缩小或者消失,监测可以停止。在一些亚洲国家,PET 是否被引进还有它的价格可能是一个问题。对于临床上评估为恶性病变的可能性低但 CT 对结节的描述并不确切的时候可以做 PET 以进一步明确。感染(例如肺结核、真菌或者寄生性疾病)和肿瘤生长缓慢(例如原位癌)可能造成 PET 结果出现假阳性或假阴性。所以,在亚洲,PET 的诊断率并不特别高,需要活检来鉴别其他因素造成的肺结节。手术活检并不同于治疗性移除所有恶性肿瘤的手术切除。一般来说,手术活检和手术切除是同时发生的,它们是肺结节诊断和治疗的金标准。可在术中行冰冻切片,如果是恶性,行肺叶切除。在亚洲,因为良性疾病(如肺结核)的发生率较高,连续影像学监测发现结节大小改变,并不能很自信地诊断其为恶性病变。对于怀疑为恶性的结节,手术切除仍然是诊断的金标准。临床医生需要根据患者的意愿,充分评估患者健康状况和适用程度推荐患者行手术治疗。外科手术推荐微创的胸腔镜手术以减低术后并发症。在亚洲国家,患者个人、患者家庭成员还有医生在决定中的角色与西方国家大有不同。临床医生在作出决定前应该充分考虑当地的文化环境。还要在制定处理方案的时候考虑到患者的意愿。专家小组注意到,在很多亚洲国家,临床医生被期望提供多个方案去引导患者做出选择。多学科小组的成立可以帮助推荐处理方法的选择。没有证据支持修改 ACCP 的推荐。3. 直径﹤8 mm 的实性结节(图 3)≦8 mm 的实性肿瘤虽然为恶性病变的可能性很低,但不能完全排除。此外,由于环境危险因素的影响,以高风险和低风险分类的二分法在亚洲很多地区不适用。事实上,专家小组推荐增加对肺部小结节监测频率和延长监测时间(根据临床判断和患者意愿延长到 3 年以上)而不是 ACCP 所推荐的类似于「高风险组」的算法。这样的做法旨在发现结节的大小变化和确定结节是否稳定。一个泰国的研究发现,≦8 mm 的结节肺结核的发生率很高,特别是 4.5-11 mm 的小结节。这告诉我们要充分考虑在亚洲地区非恶性病变引起的肺结节。低剂量 CT 扫描随访成为可能性。代谢细胞的数量过少限制了 PET 对≦8 mm 的结节诊断率。与 ACCP 指南相比,亚洲专家小组建议对高风险肺结节患者实行长期 CT 监测(3 年以上)。尽管专家小组承认没有证据支持之一理论,这一推荐是根据早期腺癌的自然发展史。图 3 直径﹤8 mm 实性结节的处理策略4. 非实性(磨玻璃)结节(图 4)非实性结节中普通的肺组织和血管可见。癌前病变非典型腺瘤样增生表现为磨玻璃样,可能多年后才转变为恶性。专家小组指出,磨玻璃结节有癌前病变和恶性病变的可能性,为采取积极的措施进行监测提供论据。此外,磨玻璃结节很多都随着时间消失,再次证明监测方法的适用性。专家小组同意对非实性结节进行长期随访监测,但这还没有证据支持。但基于早期肺腺癌的生长特性,可考虑 3 年以上的长期监测5. 部分实性结节(图 4)部分实性结节是指拥有实性成分,大磨玻璃成分﹥50%。若 CT 显示实性成分较多,浸润性病变的可能性越大。尽管经验性抗菌治疗会给病人带来一定的伤害,但专家小组认为,如果患者肺癌的发病风险低,如抗结核治疗等抗菌治疗可以考虑选择。图 4 非实性(磨玻璃)和部分实性结节的诊疗流程专家小组认为,在某些临床情况下,对较大的结节(> 8 mm)每 3 月一次的 CT 复查评估可能造成诊断的延误。在这种情况下,可考虑性即时的介入治疗。对于选择非手术的活检还是手术切除,应该根据各个中心专业水平,患者的身体状况还有患者的意愿来选择。若果可以,建议在术前行 PET 对疾病进行分期。6. 一个或多个结节对于在 CT 上发现一个或者多个肺结节,应该考虑所有结为恶性的可能性。尽管 PET 很难对≦8 mm 的结节进行描述,但术前 PET 有助于指导进一步评估。ENB 等新技术可以对外周的多个小病灶同时进行活检和病理评估。7. 介入性检查随着许多技术的出现并完善,肺结节的确诊和处理的手段大大增加。可用的收到可以大致分为影像学、细胞学、传统 / 改进的支气管镜技术还有手术 / 非手术活检技术。每一种方法都有其优缺点还有诊断率(表 2)。相对于单独使用某种方法,几种方法的结合有助于增加诊断的精确度并可能降低风险。表 2 目前对肺结节的诊断技术EBUS = 气管镜腔内超声检查; ENB = 电磁导航支气管镜检查; ROSE = 快速病理评估; TBB = 经支气管 (肺) 活检; TBNA = 经支气管针吸活检术; TTNA = 肺穿刺针;VNB = 虚拟支气管镜检查在综合考虑患者情况、肺结节的特征、费用还用当地的医疗水平等情况下,使用哪种诊断方法需要考虑将诊断率最大化,将并发症发生率最低化。连续 CT 监测适用于以下情况(见推荐,1.2, 2.3, 2.4, 3.1, 3.2, 4.1, 4.2, 5.1)细胞学方法包括痰细胞学检测还有通过非手术活检方法获得的细胞样本。痰细胞学检查是一项非侵入性的检查,但对外周的病变诊断率较低(总体敏感度为 49%)。非手术活检的推荐详见推荐 2.7,5.2 和图 3,手术活检推荐详见推荐 2.8,5.2 和图 3。非手术活检包括传统的技术例如经皮肺穿刺活检(TTNB)还有传统支气管镜联合经支气管穿刺活检。TTNB 对于外周型 < 1.5 cm 的结节诊断率≧90%。敏感度受结节大小,穿刺针的大小,穿刺的次数还有现场病理学检测的影响。但有肺部基础疾病的患者不能忍受 TTNB 所带来的并发症,特别是气胸。据报道,过去十年 TTNB 引起的气胸的发生率有 9-54%,一个大型的横断面分析报告指出,气胸的发生风险为 15%。如果考虑手术活检,应该选用胸腔镜下楔形切除。但若果结节 < 1 cm,位置较深,为半实性就难以定位。手术活检的诊断率可以通过无线介导、亚甲蓝和超声等手段提高(表 2)。除了能病变活检,ENB 可以同时使用染料标记标记病变部位,这样就能即时行手术切除病灶。对于可切除的非小细胞肺癌,应该行肺叶切除及系统淋巴结清扫。对于 < 2 cm 的外周病变,可以选择亚肺叶切除,包括肺段切除和楔形切除并行纵膈淋巴结采样。但此方法需要当前进行的前瞻性随机临床试验结果验证。讨论这些临床实践指南满足了对肺结节的评价的需要,尤其是考虑到许多亚洲国家肺癌发病率的增加与肺癌的独特的特点。亚洲肺疾病和胸外科多学科专家小组结合亚洲患者的特点对美国胸科医师学会(ACCP)制定的肺结节评估指南作了适当的调整。同时强调了由于亚洲地区肺结核高发,不宜用 PET 进行筛查,适合使用非手术活检优于手术性诊断(恶性可能性大)还有定期监测(恶性可能性小)。由于吸烟,空气污染,煤炭和生物燃料的使用等多重危险因素,肺癌在许多亚洲国家的发病率有上升趋势。与西方国家相比,亚洲地区吸烟率才刚刚达到顶峰或者仍在上升,这意味着其还继续成为肺癌的主要危险因素。中国 2010 年男性的吸烟率大概有 52.9%。在韩国,吸烟者患肺癌的风险是非吸烟者的 4.2 倍。因此,韩国制定了指南对年龄 5074 岁的重度吸烟者进行筛查,指南包括在筛查过程中检测到的肺结节评估的指导。在亚洲部分人群,特别是中国和韩国男性,肺癌的发病率要比移民到西方国家的亚洲男性要高。这种可能反映了亚洲地区吸烟率较高还有其他风险因素的存在。空气污染被认为是全球引起死亡的最主要环境因素,它对 DNA 诱变效应导致多种癌症的发生,其中包括肺癌。空气污染在亚洲地区很普遍,在有些国家中还很严重,特别是在中国和印度的大城市中。职业暴露于石棉或其他致癌物质可以增加肺癌的风险。除了室外空气污染,由于使用煤还有生物燃料造成的室内空气污染造成了呼吸道感染、慢性呼吸道疾病和肺癌,尤其是那些有肺结核,慢性阻塞性肺疾病等慢性肺疾病史的患者。相比西方国家女性,没有吸烟史的女性患肺癌的风险也有所增加。肺腺癌是亚洲最常见的肺癌类型,尤其是女性,这可能反映了遗传差异和其他危险因素。最近的一项中国大陆,韩国,日本,新加坡,台湾和香港不吸烟的亚洲女性全基因组关联分析,确定了三个新的易感基因位点并证实与其他位点相关联。女性较男性更容易患有肺癌,这可能涉及功能基因间的差异。亚洲女性患肺癌的危险因素包括煤和生物燃料的使用、被动吸烟,炊烟还有二手烟。从广义上讲,大多数亚洲国家对肺结节的诊断和处理都与西方国家大有不同。然而,肺结节的评估,很可能是由亚洲和西方之间的差异,亚洲不同国家间的差异,还有国家不同地区间的差异导致。这些差别主要涉及在亚洲(ⅰ)上述讨论的肺癌的危险因素(ⅱ)肉芽肿,感染性疾病,可混淆诊断(iii)肺癌的遗传倾向。此外,可用的设备,宗教和文化信仰和家庭的决策也可能影响肺结节的评价。专家小组意识到在亚洲的几个国家中已经存在对肺结节的评估指南。上述指南并不是要替代这些当地指南,而是针对亚洲的情况,对其进行补充。这里其中一项与 ACCP 指南不同的推荐是把 CT 连续监测的时间延长到 3 年以上。专家小组没有足够的证据支持这一推荐,它是基于亚洲的许多国家肺癌的总体风险较高提出的。该小组的专家也承认,反复暴露于电离辐射的风险不容小觑。另一个重要的与 APCC 指南不同点涉及初诊使用定量评估,预测恶性的概率。APCC 所推荐的如 Mayo Clinic 模型因为某些关键因素并不适用于亚洲人群。这些因素包括肉芽肿病及其他感染性疾病发生率高,空气污染严重,非吸烟肺癌患者较多。专家小组认为不同的国家建立一个当地的验证预测模型。当前,中国正在用自己国家的数据更新 Mayo Clinic 预测模型。上述修订的临床实践指南有几个关键的局限点。最主要的一个是没有数据支持对 ACCP 推荐的修改。专家小组承认了根据这些推荐的最终实践者的反馈更新指南的重要性。在这个方面,调整指南的过程中显示出现有证据不足,建议当地进一步研究。其次,国家之间还有地域间的广泛差异使得指南难以在整个亚洲地区广泛适用。因此,临床医生应该充分考虑现有资源、专业知识等方面的限制,适当采取某些推荐应用到自己的临床实践。总之,这个指南是亚洲肺疾病和胸外科多学科专家小组在 ACCP 制定的肺结节评估指南的基础上,经过共识制定临床实践指南。 大多数 ACCP 指南所提出的建议广泛适用于亚洲地区,做出的修改主要是解决非吸烟者所患肺癌的风险较西方国家高还有亚洲地区的感染性疾病发病率较高。另外,专家小组推荐未来的指南使用 4 mm 为分界点(实性结节 4 mm,非实性结节 5 mm)以便更好地实施。指南推荐:1. 性质未明肺结1.1 推荐:在胸片上新发现一个性质未明肺结节时,回顾该患者之前做的影像检查。1.2 推荐:对于大小在 2 年内变化不明显的性质未明的肺结节,高危患者每年做 CT 筛查时间超过 2 年1.3 推荐:对于胸片发现性质未明的肺结节患者,行低剂量螺旋 CT(最好是薄层)了解结节的特征,评估其为恶性的可能性(表 1)2. > 8 mm 性质未明的实性结节2.1 推荐:对于 > 8 mm 性质未明的实性结节,应该由一个中心的多学科处理。这个中心应有 CT/PET,良性病变的诊断能力(如肺结核)还有活检(手术或微创)2.2 推荐:对于 > 8 mm 性质未明的实性结节,根据临床判断其为恶性的可能性。如果可能,使用一个有适当区域注意事项说明的验证模型做定量评估。2.3 推荐:对于 > 8 mm 性质未明的实性结节,有一下情况应该用 CT 进行监测:临床上预测其为恶性的概率很低 (<5%)活检阴性,PET 评价病灶非高代谢尽管充分了解疾病有进展的风险,患者更愿意这种非侵入性的处理方式2.4 推荐:对于 > 8 mm 性质未明的实性结节,需要在 3-6 月,9-12 月,18-24 月进行连续的薄层 CT 的监测,之后,根据临床的判断和患者的意愿每年做一次。2.5 推荐:对于 > 8 mm,其为恶性的可能性为 5-60%(中度)的性质未明的实性结节,在手术活检或继续做影像学监测前,可以考虑做 PET 进一步明确结节的特征。注意不能用 PET 进行筛查。2.6 推荐:对于 > 8 mm,其为恶性的可能性 > 60%(高)的性质未明的实性结节,功能性成像技术对术前进行分期可能比对结节的特征描述更重要。2.7 推荐:对于 > 8 mm 性质未明的实性结节,在以下情况下进行非手术活检:临床上预测其为恶性病变的可能性为中度(5-60%)PET 显示结节高代谢非手术活检结果为可疑阳性患者已充分了解介入性诊断的程序2.8 推荐:如果结节为恶性的可能性大,PET 可以进行术前分期,查找之前没有被发现的转移。2.9 推荐:对于 > 8 mm 性质未明的实性结节,若患者选择手术活检,推荐行微创手术2.10 推荐:对于 > 8 mm 性质未明的实性结节,临床医生在作出处理前应该充分考虑患者的经济情况3. 直径﹤8 mm 的实性结节3.1 推荐:对于≦8 mm 肺癌风险较低的实性结节,行 CT 对结节的大小进行监测:≦4 mm 的结节,根据患者的意愿和临床的判断,考虑进行每年的 CT 检查﹥4 mm,≦6 mm 的结节,如果大小稳定,根据患者的意愿和临床的判断,考虑行每年行低剂量螺旋 CT 检查对其重新评估。﹥6 mm,≦8 mm 的结节,如果大小稳定,根据患者的意愿和临床的判断,在 6 月、18-24 月行低剂量螺旋 CT 检查对其重新评估。3.2 推荐:对于≦8 mm 肺癌高风险的实性结节,结节的大小行 CT 进行监测:≦4 mm 的结节,12 个月后复查 CT,之后根据患者的意愿和临床的判断,考虑进行每年的 CT 检查﹥4 mm,≦6 mm 的结节,6-12 个月, 18-24 个月时行 CT 对其重新评估,若无明显变化,根据患者的意愿和临床的判断,每年复查。﹥6 mm,≦8 mm 的结节,在 3 个月,6 个月,12 个月时行 CT 对其重新评估,如果大小稳定,根据患者的意愿和临床的判断,每年复查。4. 非实性(磨玻璃)结节(图 4)4.1 推荐:对于≦5 mm 的非实性(纯磨玻璃)结节,根据患者的意愿和临床的判断,每年行 CT 检查监测。4.2 推荐:对于>5 mm 的非实性(纯磨玻璃)结节,至少 3 年内每年做 CT 对结节进行再次评估,之后根据患者的意愿和临床的判断,每年行 CT 检查监测。5. 部分实性结节(图 4)5.1 推荐:≦8 mm 的部分结节,在 3 个月,12 个月,24 个月时行低剂量螺旋 CT 对其重新评估,如果结节稳定,根据患者的意愿和临床的判断,每年复查。若有细菌感染的征象,应经验性地使用抗生素进行排查。5.2 推荐:>8 mm 的部分结节,每 3 个月行低剂量螺旋 CT 对其重新评估,若有细菌感染的征象,应经验性地使用抗生素进行排查。对于 3 个月后仍然存在的结节,可考虑行非手术活检和 / 或外科手术,在术前可行 PET 对其进行分期。6. 一个或多个结节6.1 推荐:除一个主要的结节外,还伴有一个或一个以上的其他结节,专家小组建议对每个结节进行单独评估,不排除根治性治疗,酌情考虑病理学确认是否为转移。7. 介入性检查7.1 推荐:当选择非手术活检时,选择哪种方法应考虑一下方面:结节靠近胸壁或者位置较深,特别是不需要穿过肺裂,周围无肺气肿的情况下,可考虑使用 TTNA 或 TTNB结节靠近支气管,可见支气管征,或气胸高危患者可考虑使用支气管镜如果条件允许,可使用改良的支气管镜检查,特别是在结节较小还有结节周围有肺气肿的情况。
王保收 主任医师 开封市中心医院 胸外科4705人已读 - 医学科普 2020版NCCN肺癌筛查指南
从2020 版NCCN 指南推荐来看对于非实性结节(纯磨玻璃)更偏向于随访,而非手术干预,将随访的阈值定为2cm,主要原因是随访过程中不消失或增大的非实性结节术后病理大多为原位和微浸润腺癌,完整切除后的5年生存率几乎为100%,与长期的临床研究相符。 --Mark.Shen 肺癌已成为全球主要恶性肿瘤,其发病率不断升高。有效的筛查可以更早地发现肺癌,使无症状性肺癌及时发现,提供早期干预,从而降低肺癌的死亡率。NCCN自2011年开始制定和公布肺癌筛查的指南,每年至少更新一版。为了更好的理解并应用于临床实践,来自浙江省台州医院胸外科的同道对2020版NCCN肺癌筛查指南进行翻译并整理,内容如下: NCCN肺癌筛查小组指南更新摘要 风险评估(LCS-1) 肺癌的危险因素肺癌的危险因素包括:吸烟(包括二手烟),职业性致癌物质的暴露(砷、铬、石棉、镍、镉、铍、二氧化硅、柴油废气、煤油烟等),氡的暴露,既往恶性肿瘤病史(如肺癌、淋巴瘤、吸烟相关恶性肿瘤,如:膀胱癌及头颈部肿瘤等),肺癌家族史,肺部相关疾病史(慢性阻塞性肺疾病、肺纤维化),激素替代治疗(女性)。 高危险组1的入组标准:55~77岁;30包/年或以上吸烟史;具有吸烟史,而戒烟时间短于15年。新版中将年龄从74岁增加到了77岁,主要考虑到人群预期寿命。 高危险组2的入组标准:50岁或者以上;20包/年或以上吸烟史;有至少一条高危因素(二手烟除外)。对于此类人群,指南推荐进行低剂量CT筛查。延长的原因。对于此类人群,指南推荐进行低剂量CT筛查,且即使首次检查为阴性或者结节大小未达到进一步检查标准,仍然推荐每年进行低剂量CT筛查。 中危险组的入组标准:50岁或者以上;20包/年或以上吸烟史(包括二手烟暴露);无其他高危因素。指南不推荐对此类患者进行低剂量CT筛查。 低危险组的入组标准:50岁以下;20包/年以下吸烟史。指南不推荐对此类患者进行低剂量CT筛查。 注解: 1.肺癌筛查适用于肺癌的高危潜在治疗对象。胸部x光不推荐用于肺癌筛查。 2.所有目前吸烟的人都应该被劝告戒烟,既往吸烟者应该被劝告保持戒烟。 3.肺癌筛查不应被认为是戒烟的替代品。吸烟史应记录吸烟者的既往暴露程度(以包年计)和已戒烟时长。 4.被特别识别为肺部致癌物为:二氧化硅、镉、石棉、砷、铍、铬、柴油烟雾、镍、煤烟和烟尘。 5.在肺癌、淋巴瘤、头颈癌或吸烟相关癌症的幸存者中,新发原发性肺癌的风险提升。 6.二手烟暴露的致癌性异质性较强,且该暴露可变性较大,风险增加的证据各不相同。因此,二手烟并不独立地被认为是推荐肺癌筛查的一个充分危险因素。 7.虽然随机试验证据支持筛查截至77岁,但是否需要对77岁以上的人群实行筛查,尚无定论。目前认为,只要目标还是潜在的肺癌治疗对象,就可以纳入筛查人群。 8.所有的筛查和随访胸部CT都应在低剂量(100-120kVp和40-60 mAs或更低)下进行,除非需行增强CT以评估纵隔异常或淋巴结。 低剂量CT首次发现病灶的随访策略(LCS 2-5) 筛查结果(LCS-2) LDCT初步筛查时为实性结节(LCS-3) LDCT初步筛查为部分实体结节(LCS-4) LDCT初步筛查为非实性结节(LCS-5) 良性和感染的病灶 指南推荐在1~3个月内复查低剂量CT,如病灶完全消散则每年进行低剂量CT筛查;如病灶正在消散则3~6个月后复查低剂量CT,直至其稳定后,每年复查低剂量CT;如病灶持续存在,或者首次发现即考虑恶性可能,则根据首次发现病灶的不同类型,NCCN肺癌筛查指南制定了不同的随访策略。 实性结节性病灶 根据结节大小,分别采取不同的随访策略。(1)对于≤5mm的实性结节,指南推荐每年进行低剂量CT随访,直至筛查对象不再为肺癌潜在患者(关于随访终止时间目前尚无明确定论)。(2)对于6~7mm的实性结节,指南推荐间隔6个月进行低剂量CT随访。(3)对于8~14mm的实性结节,指南推荐间隔3个月进行低剂量CT随访或者直接进行正电子发射计算机断层显像(PET-CT)筛查(PET-CT对15mm的实性结节,指南推荐进行常规剂量增强CT和/或PET-CT筛查,同样高度怀疑恶性者,考虑活检或者手术切除,而恶性低可能性者推荐间隔3个月进行低剂量CT随访。(5)对于支气管腔内实性结节,建议1个月内复查低剂量CT,如无变化,建议行支气管镜检查。 部分实性结节性病灶 根据结节大小,分别采取不同的随访策略。(1)对于≤5mm的部分实性结节,指南推荐每年进行低剂量CT随访,直至筛查对象不再为肺癌潜在患者(关于随访终止时间目前尚无明确定论)。(2)对于≥6mm,实性成分≤5mm的部分实性结节,指南推荐间隔6个月进行低剂量CT随访。(3)对于≥6mm,实性成分为6~7mm的部分实性结节,指南推荐间隔3个月进行低剂量CT随访或者直接进行PET-CT筛查,对于PET-CT高度怀疑恶性者,考虑活检或者手术切除,而恶性低可能性者推荐间隔3个月进行低剂量CT随访。(4)对于实性成分≥8mm,无论其结节大小,指南推荐进行常规剂量增强CT和/或PET-CT筛查,高度怀疑恶性者,考虑活检或者手术切除,而恶性低可能性者推荐间隔3个月进行低剂量CT随访。 非实性结节(磨玻璃结节)病灶 根据结节大小,分别采取不同的随访策略。(1)对于≤19mm的非实性结节,指南推荐每年进行低剂量CT随访,直至筛查对象不再为肺癌潜在患者(关于随访终止时间目前尚无明确定论)。(2)对于≥20mm的非实性结节,指南推荐间隔6个月进行低剂量CT随访。值得注意的是,即使因高度怀疑为恶性肿瘤行活检或手术切除明确为良性,此类人群仍然需要每年低剂量CT筛查,直至筛查对象不再为肺癌潜在患者(关于随访终止时间目前尚无明确定论)。 注解: 1.应在肺窗上测量结节大小,并记录为四舍五入到最接近整数的平均直径;对于球形结节,只需要测量一个直径。平均直径是结节的最长直径和垂直直径的平均值。 2.PET-CT对实性成分小于8 mm的结节和靠近膈肌的小结节的敏感性较低。PET/CT只是确定结节是否具有高肺癌风险的多个标准中的一个考虑因素。在真菌病流行地区,PET-CT假阳性率较高。 3.如一次活检未能完成诊断,并对癌症仍抱有高度怀疑,建议重复活检/手术切除或短周期随访(3个月)。 4.活检组织样本量需要足够用于组织学和分子学检测。 5.需对所有非实性结节进行薄层(1.5mm),根据其大小,采取不同的随访策略。(1)对于≤7mm者,指南推荐间隔3个月进行低剂量CT随访。(2)对于≥8mm者,指南推荐进行常规剂量增强CT和/或PET-CT筛查,高度怀疑恶性者,考虑活检或者手术切除,而恶性低可能性者推荐间隔3个月进行低剂量CT随访。 无变化的部分实性结节 对于随访过程中无变化的部分实性结节,根据其大小,采取不同的随访策略。(1)对于≤5mm,或者≥6mm,实性成分6~7mm的部分实性结节,指南推荐每年进行低剂量CT随访。(2)对于≥6mm,实性成分≥8mm的部分实性结节,指南推荐间隔6个月进行低剂量CT随访,如无变化则每年进行一次筛查;或者直接进行PET-CT筛查,对于PET-CT高度怀疑恶性者,考虑活检或者手术切除。(3)对于随访过程中始终无变化的部分实性结节,则继续每年低剂量CT筛查。 增大或新增部分实性结节 对于随访过程中增大(实性增大>1.5mm)或者新增的部分实性结节,根据其大小,采取不同的随访策略。(1)对于≤5mm的新增部分实性结节,指南推荐间隔6个月进行低剂量CT随访。(2)对于≥6mm,实性成分≤3mm的部分实性结节,指南推荐间隔3个月进行低剂量CT随访。(3)对于实性成分≥4mm的部分实性结节,指南推荐进行常规剂量增强CT和/或PET-CT筛查,高度怀疑恶性者,考虑活检或者手术切除,而恶性低可能性者推荐间隔3个月进行低剂量CT随访。 无变化后新增非实性结节 对于随访过程中无变化后新增的非实性结节,根据其大小,采取不同的随访策略。(1)对于≤19mm的非实性结节,指南推荐每年进行低剂量CT随访。(2)对于≥20mm的非实性结节,指南推荐间隔6个月进行低剂量CT随访,如无变化,改为每年进行低剂量CT随访。 增大的非实性结节 对于随访过程中增大的非实性结节(增大>1.5mm),根据其大小,采取不同的随访策略。(1)对于≤19mm的非实性结节,指南推荐间隔6个月进行低剂量CT随访。(2)对于≥20mm的非实性结节,指南推荐间隔6个月进行低剂量CT随访,也可以考虑进行病理活检或者手术切除明确病理。值得注意的是,即使因高度怀疑为恶性肿瘤行活检或手术切除明确为良性,此类人群仍然需要每年进行低剂量CT筛查,直至筛查对象不再为肺癌潜在患者(关于随访终止时间目前尚无明确定论)。 注解: 1.病灶大小迅速增加应提高对炎症病因或除非小细胞肺癌以外的恶性肿瘤的怀疑。 2.新发结节定义为平均直径≥3 mm。 目前对于多发结节的随访,主要是根据优势病灶(体积最大或者实性成分最多)的情况采取相应的随访策略。 肺癌筛查的利弊 获益: (1)降低肺癌死亡率(有效的肺部筛查每年可防止超过12,000例肺癌过早死亡); (2)提高生活质量:降低疾病相关死亡率、降低治疗相关死亡率、促使筛查人群改变影响健康的生活方式、减少焦虑和心理负担; (3)发现其他潜在的重大健康风险(例如甲状腺结节、严重但无症状的冠心病、肾上极早期肾癌、主动脉瘤、乳腺癌)。 风险: (1)假阳性结果导致不必要的检查甚至是侵入性的干预(包括手术),增加了经济负担,同时也增加了患者精神上的痛苦,降低了患者生活质量; (2)假阴性结果可能延误肺癌的诊断,耽误患者的治疗; (3)对于小的侵袭性肿瘤的无效检查(可能已经发生转移,导致对延长生存时间无意义的随访); (4)对于惰性病灶的无效检查,此类病灶无需治疗也不会对患者生命产生任何影响; (6)没有必要的放射暴露; (7)诊断操作中的并发症。
 沈建飞 副主任医师 台州医院 心胸外科3920人已读
沈建飞 副主任医师 台州医院 心胸外科3920人已读 - 论文精选 临床早期NSCLC不建议行淋巴结采样
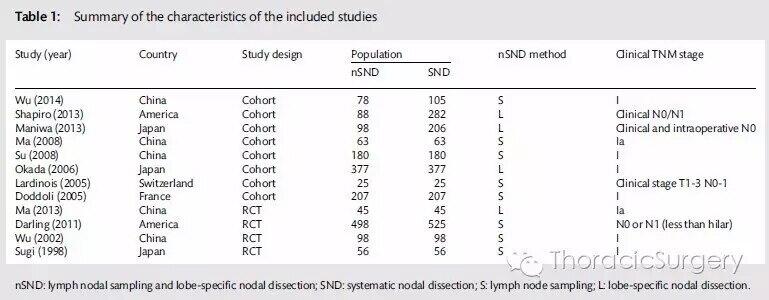
随着影像学和诊断技术的发展,临床早期非小细胞肺癌(NSCLC)患者的检出数与日俱增。国家综合癌症网络(NCCN)指南推荐,临床早期NSCLC的治疗首选肺叶切除术+系统性淋巴结清扫(SND)。针对不同区域的纵隔淋巴结切除,如淋巴结采样(LNS)和肺叶特异性淋巴结切除(L-SND)。某前瞻性研究比较SND与其他限制性淋巴结切除,其结果证实SND组并没有生存获益。 换言之,目前临床早期NSCLC不同淋巴结切除方法及其预后意义仍存在争议。鉴于此,来自浙大一附院的胡坚教授等完成了该项系统回顾和荟萃分析,通过随机效应模型的方法分析比较SND、LNS和L-SND三种不同淋巴结切除方式治疗临床早期NSCLC的预后,文章发表于Eur J Cardiothorac Surg杂志上。 该荟萃分析检索了PubMed、OVID、EBSCO和Springer四大数据库,截止至2015年8月的英文文献。文章纳入标准如下:(i)有对比SND与LNS或L-SND治疗NSCLC的临床疗效;(ii)临床分期N2(-)的NSCLC手术预后具体数据或可据其计算HR;(iii)研究相比较的每组NSCLC患者大于20例;(iv)过去20年内已发表的英文文献。 图1,荟萃分析纳入12项研究的数据概况 本研究纳入12项研究,其中4项为前瞻性随机对照临床研究(RCT)、8项为观察性研究,共3955例接受手术治疗的临床N2(-)期患者,SND组2142例,非SND组1813例(其中LNS(n=1215),L-SND(n=608))。观察性研究分析结果表明,SND组的总生存率(OS,HR=1.24;95%CI:1.02-1.5)和无复发生存期(RFS,HR=1.27;95%CI:1.03-1.58)两者较非SND组均有显著改善。 图2,非RCT研究和RCT研究分析结果的森林图 四项RCT研究的合并HR分析结果显示,两组患者的预后无明显差异,OS,HR=1.13,95%CI:0.94-1.35;RFS,HR=0.99,95%CI:0.82-1.19。在亚组分析中,SND组可显著改善OS(HR=1.40,95%CI:1.12-1.76)和RFS(HR=1.5;95%CI:1.09-2.08)。然而,SND组和L-SND组两者之间无显著差异,OS(HR=1.02;95%CI:0.66-1.57);RFS(HR=1.11;95%CI:0.87-1.42。 图3,SND组和L-SND组患者OS与RFS的分析结果森林图 总之,从上述研究结果看来,临床早期NSCLC患者采取LNS方式进行治疗其预后较差,不可取。而L-SND与SND两者的预后差异不大。但是,以上结果和结论还需未来的进一步研究去证实。 文章题目:Lymphadenectomy for clinical early-stage non-small-cell lung cancer: asystematic review and meta-analysis (PMID: 27107044)
 沈建飞 副主任医师 台州医院 心胸外科627人已读
沈建飞 副主任医师 台州医院 心胸外科627人已读 - 学术前沿 浸润性肺腺癌分级系统(基于病理亚型):IASLC病理委员会提议
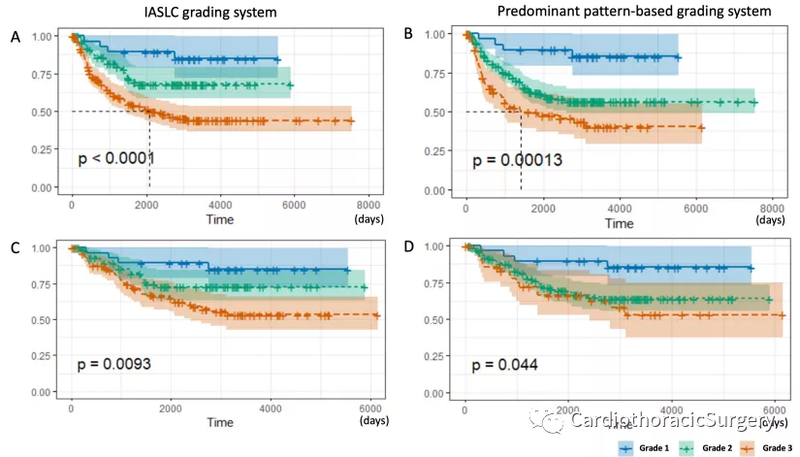
摘要 背景:肺腺癌的分级系统尚未建立。IASLC病理学会评估了一套与预后相关的组织学标准,旨在建立浸润性肺腺癌的分级系统。 设计:进行了一项涉及多个浸润性肺腺癌队列的多机构研究。一组284例I期肺腺癌被用作研究队列,以确定与患者预后相关的组织学特征(无复发生存期(RFS)和总生存期[OS])。采用ROC曲线分析筛选出最佳模型,并在独立队列中进行验证(n=212)和测试(n=300,包括I-III期患者)。用Kappa统计量评估模型的可重复性。 结果:最佳模型(RFS的AUC=0.749,OS的AUC=0.787)是以高级别为主的组织学模式的组合,后者的临界值为20%。该模型包括:1级:以贴壁为主的肿瘤;2级:腺泡或乳头状为主的肿瘤,两者的高级别模式均不超过20%;3级:任何具有20%或以上高级别模式(实体、微乳头和/或复合腺体)的肿瘤。在验证(RFS和OS的AUC值分别为0.732和0.787)和测试队列(RFS和OS的AUC值分别为0.690和0.743)中也看到了类似的结果,证实了模型的预测价值。观察者间一致性良好(k=0.617)。 结论:基于主要和高级别模式的分级系统有助于浸润性肺腺癌预测预后。 引言 肿瘤分级一直是病理学评估的传统组成部分,并为许多器官系统的治疗和患者管理提供指导[1-5]。然而,对于浸润性肺腺癌的分级系统还没有达成共识。2015年世界卫生组织(WHO)对肺腺癌的分类[6]发现与预后相关,并将肺腺癌分为三个预后组,即低级别(以贴壁为主)、中级别(腺泡或乳头为主)和高级别(实性或微乳头为主)组。也有人建议,根据主要模式的分类和分层可以预测辅助化疗的反应[7]。 肺腺癌在组织学上是异质性的,呈现出多种模式和比例的组合。当仅按主要类型分类时,腺泡亚型是最常见的(约占40-50%),预后多样[8-12]。除了五种主要的组织学模式外,肺部还发现了其他几种模式,在其他器官的腺癌中也发现了这种模式[13]。这些类型包括筛状(定义为有筛孔样的肿瘤细胞巢)和融合腺体(定义为形态不佳的融合腺体,无间质,或呈带状结构,边界不规则,单细胞浸润间质)。2015年WHO分类承认肺腺癌中的筛状型,但决定不创建一个新的亚型,而是将其描述为肺腺泡亚型的高级别模式的一部分[6],这些复杂的腺体模式(高级别腺泡)已经发现与高有丝分裂率、肿瘤坏死和淋巴管浸润有关[14,15]。此外,目前的证据一致认为,这些复杂的腺体模式与高级别组织学类型(实性和微乳头状)的预后很差[11,14-19]。然而,由于缺乏对这些模式的认识,可能导致肿瘤分类的不确定性和较差的重复性,因为一些研究人员可能已经将这些模式归类为中级(腺泡)或高度分级(实性)。因此,重要的是要识别这些“非传统模式”,并将它们与常规的腺泡模式分开归类为复杂腺体。 最近的研究建议包括许多其他病理特征,如次级组织学类型[20]、核分级[21-23]、有丝分裂分级[22-24]、是否存在通过气隙扩散(STA)[25-29]和坏死[30,31]列为主要的模式分类,以改进分级方案。所有这些其他的组织学特征都被证明具有预后价值,然而,大多数研究将这些特征作为一个单个参数进行评估,没有考虑到肺腺癌的异质性。目前还没有系统的方法来评估和将多个建议的预后因素纳入分级系统。通过分级系统补充肺腺癌的分类将有助于定义预后人群,并为肺腺癌患者的预后分层提供一条共同的途径,这些患者可能受益于不断变化的管理和治疗方案的变化。 因此,IASLC病理学委员会进行了一项系统的研究,以评估一系列被描述为预后指标的组织学特征,并建立一个已切除的浸润性肺腺癌的分级系统。 材料与方法 研究队列 评估了一项涉及多个明确注释的已切除肺腺癌队列的多机构研究。所有病例均按第8版AJCC癌症分期手册[1]进行分期,并进行至少5年的随访。这项研究包括了四个独立的数据集。每个数据集收集均获得各自机构审查委员会(IRB)的批准。美国数据集是根据HIPPA的规定收集的。 一个由284例I期病例组成的队列(New York University Langone Health, NY, USA)被用作研究队列,用于评估构建分级系统所使用的最佳参数。研究结果在212例I期病例(Massachusetts General Hospital, MA, USA)和另一组300例I-III期病例(Brigham and Women’s Hospital, MA, USA and St Vincent’s Hospital, Melbourne, Australia)中得到验证。表1显示了所有队列的人口统计信息。 组织学评价 研究和验证队列中的病例由提交的病理学家(ALM,MMK)审查,并评估下列组织学参数。测试队列中的案例未专门针对本研究进行审核,因为它们代表了提供者机构(LMS,PAR)的历史集合。 1. 根据当前的WHO肺肿瘤分类[6],在所有研究和验证队列病例中,对所有存在的模式进行半定量估计,并以5%的增量递增进行全面的组织学分型[6]。包括了WHO确定的所有五种模式,以及筛状腺和融合腺(复合腺体模式)等非传统模式,总计100%。图1说明了复杂腺体模式。原位腺癌、微浸润性腺癌、多灶性腺癌、浸润性粘液腺癌(IMA)和其他变异型腺癌均被排除在本研究之外。 2. 核分级的确定如前所述[21-23]。1级:圆形,规则的细胞核,染色质均匀分散,无明显核仁,大小可达淋巴细胞的2-3倍;2级:圆形,轻度不规则,极小的多形核,无明显核仁,大小可达淋巴细胞的2-3倍;3级:多形核,突出的核仁,大于淋巴细胞大小的5倍(补充图1)。 3. 有丝分裂分级如前所述[22,23],即1级:0-1个有丝分裂图/10高倍视野;2级:2-4个有丝分裂图/10高倍视野;3级:≥5个有丝分裂图/10高倍视野。 4. 细胞学分级定义为低级别:细胞多形性低,细胞体积小;高级别:细胞多形性高,细胞体积大(补充图1)。 5. 热点判定:鉴于肺腺癌的异质性,在“热点”(最高级别的区域)记录细胞核分级、有丝分裂分级和细胞学分级,并记录相应的热点组织学模式。 6. 如先前报道[25]所定义的那样,通过空气空间(STAS)传播的肿瘤细胞在主要肿瘤边缘以外的空气中形成微乳头状簇、实体巢或单个细胞。STAS被记录为存在或不存在。 7. 肿瘤内坏死也被记录为存在或不存在。 模型建设 由于主要模式用于腺癌的分类,并按预后分组显示一致的分层,因此主要模式被用作模型的基础。此外,就如何最好地代表组织学特征以实现最佳预后判断,对几种方法进行了评估和比较。组织学模式评估为“加权平均”,即所有模式的比例乘以其复发风险比之和,该比率分别来自于衡量复发时间与主要模式之间的相关性的Cox比例模型的系数得出;“二元模式”,其中组织学模式被视为存在或不存在,但与其比例无关,但根据先前建立的分级分配编号(1:贴壁;2:腺泡/乳头状腺;3:实性、微乳头/复合腺体)和“数字”,其中考虑了该模式的数值比例。 不同的研究已经应用不同的百分比截断值来定义预测不良患者预后所需的高级别模式的量[31-34]。因此,我们试图确定提供最佳区分性能的高级模式的百分比。用Youden‘s指数选择高级别模式百分比的最佳分界值,以获得≥85%的阳性预测值。我们使用复发和死亡作为结果,并比较了两者的临界值。最后,评估其他组织学特征(核分级、有丝分裂分级、细胞学分级、STAS和坏死)的作用。 统计分析 1.模型构建 描述性统计量以连续变量的标准差为均值,以分类变量的频度为比例。两样本t检验和卡方检验比较两组间的连续变量和分类变量。分别计算初诊至首次复发或死亡的无复发生存率(RFS)和总生存率(OS)。最后一次随访的时间用于接受审查的患者。COX比例风险回归用于预测研究队列中的复发情况。候选预测因子是组织学特征和临床特征,包括年龄、性别和病理分期。模型是通过评估每个预测变量的重要性和最小化Akaike的信息标准来选择的。通过回归系数加权的选定模型预测因子的线性组合被定义为风险得分,并应用于队列人群。我们通过确定复发和死亡的受试者工作特征(ROC)曲线下面积(AUC)值来评估预后的识别能力。此外,与AUC相似的一致性指数(C-index)被用来分别表示预测RFS和OS的辨别能力。值为0.5表示该模型没有判别能力,值为1.0表示该模型具有良好的判别能力。采用两侧P值
 沈建飞 副主任医师 台州医院 心胸外科4578人已读
沈建飞 副主任医师 台州医院 心胸外科4578人已读 - 学术前沿 Pembrolizumab治疗胸腺癌患者的长期随访结果
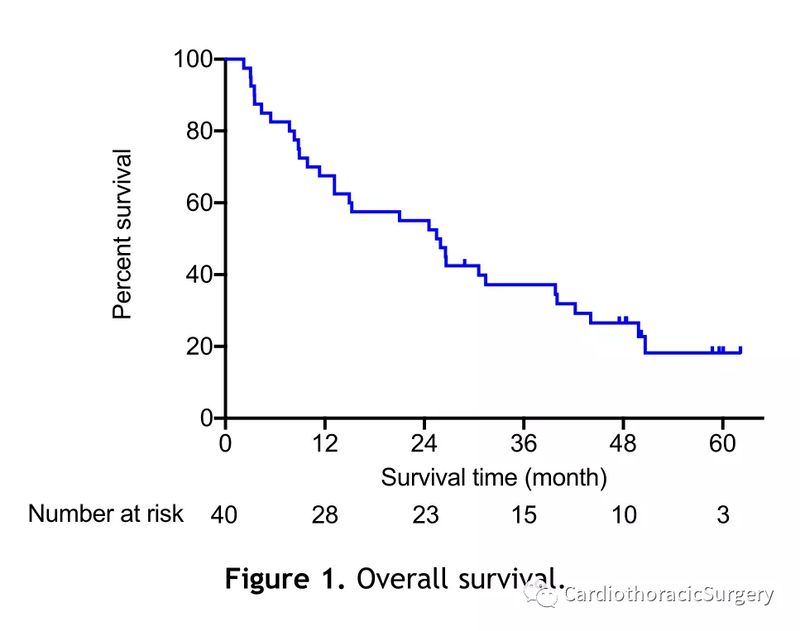
本文我们介绍了一项2期研究:pembrolizumab治疗晚期胸腺癌患者(既往治疗失败)研究的更新。反应的持续时间约为3年,中位生存期超过2年,5年生存率为18%。随着随访时间的延长,严重自身免疫性疾病的发生率(15%)并没有显著增加。Pembrolizumab能诱导胸腺癌患者产生持久反应。谨慎选择受治患者和毒性监测是必要的。 总共有40名符合条件的晚期胸腺癌患者接受了程序性细胞死亡蛋白-1 (PD-1)抗体治疗:pembrolizumab 200 mg静脉给药(每3周一次,持续2年)。 研究的初步分析发表于2年多前。中位随访时间为4.9年,所有治疗后有反应的患者(n=9)最终都发生进展。随着随访的延长,反应率没有变化(22.5%)。中位缓解持续时间为2.99年,中位无进展生存期为4.2个月,中位总生存期为2.12年(图1)。5年生存率为18%。与病情稳定(stable disease)的患者(中位生存期为2.12年)相比,应答者的生存期更长(中位生存期未达到)。 5名患者根据方案完成了2年的治疗,其中4名(患者17、11、32和22)选择继续治疗(图2)患者17和32继续治疗至病情进展之后。 患者17在进展时(治疗开始后54.2个月)接受左肺门放疗,并在最后一次随访时(治疗开始后62.9个月)仍持pembrolizumab治疗。最近的一次氟脱氧葡萄糖正电子发射断层扫描提示无活动性疾病。 四名曾终止治疗的患者在疾病进展后再次尝试pembrolizumab治疗。四名患者停用pembrolizumab的原因包括:自免性肝炎的发展(患者4)、完成2年治疗(患者5)和患者自身选择(患者11和21)。其中两名患者(患者5和11)对再次治疗有反应。 一名出现肌炎、心肌炎和重症肌无力(MG)的患者(患者28)在仅接受2个周期的pembrolizumab治疗后,近乎完全缓解持续40个月。一名患者(患者25)在治疗中断几个月后从不典型重症肌无力发展成典型的重症肌无力症状。另一名患者(患者21)2年前因疾病进展退出研究,后在pembrolizumab再次治疗后出现重症肌无力。治疗期间未观察到其他新的自身免疫性疾病。严重自身免疫性疾病的发生率为15%(40名患者中有6名),4名患者出现一种以上的严重自身免疫性疾病。 严重免疫相关不良事件(irAE)报告的中位时间是在4个周期后(范围:2-20周期)。 激素治疗的持续时间从几个星期到几个月不等,取决于个体irAE情况。从首次出现严重irAE开始计算,激素治疗的平均持续时间为2.5个月(范围为3周至>2年)。在6名患严重irAE的患者中,有2名(33.3%)需要额外联合免疫抑制治疗。对所有患重症肌无力的患者来说,重症肌无力始终是一个难以控制的问题。本研究入组时并未对乙酰胆碱酯酶抗体进行常规检测,而是在研究期间仅对怀疑有MG的患者进行了检测。 本研究结束时引入了一项修正案,以评估“epacadostat 10mg/bid联合pembrolizumab”治疗晚期胸腺癌患者的安全性和有效性(既往接受过PD-1或PD-L1治疗的患者不允许参与研究)。四名患者在研究结束前接受了治疗(尽管2期单臂研究的结果令人满意,但在联合melanoma治疗的随机试验中结果未能达到主要终点)。没有患者对这种联合治疗方案有反应,一名患者出现2级心肌炎。后研究被终止。 胸腺上皮肿瘤中免疫检查点抑制剂的其他研究尚在进行。比如韩国的一项研究中,同样pembrolizumab治疗后观察到了与我们相似的应答率、相似的自身免疫性疾病风险,但反应持续时间(中位持续时间为14.9个月)和OS(中位OS为14.5个月)比我们的研究短。在这项研究中,还包括了7名患有胸腺瘤的患者,他们患严重自身免疫性疾病的发生率要高得多(7人中有5人[71.4%])。两项研究中主要患者特征区别是种族(在韩国的研究中100%是亚洲人,而在我们的研究中是10%)。此外,我们的研究允许患者持续治疗超过2年(4名患者),并在4名尝试再治疗的患者中有2名患者治疗有效。在胸腺瘤和胸腺癌中也报道了使用avelumab的研究(一种PD-L1抑制剂),具有相似的活性,但胸腺瘤患者并发严重自身免疫性疾病的发生率高(5/7[71.4%])。一项日本的2期研究对胸腺癌患者进行nivolumab治疗,但是这项研究在观察累计15名患者后没有发现任何治疗反应,随后终止。在这项研究中,两名患者(13.3%)出现了严重的irAEs。 目前有几项将免疫检查点抑制剂作为单一药物或联合药物的研究正在进行(表1)。目前其他备选治疗策略还有血管生成抑制剂,比如sunitinib和lenvatinib。具体联合疗法尚在研究当中。 总之,在这项研究中,单用pembrolizumab在主要为高PD-L1表达的患者中产生了持久的反应,但所有患者最后均复发。为了提高基于PD-1或PD-L1的治疗在胸腺恶性肿瘤治疗中的疗效和安全性,需要对联合疗法进一步研究,并寻找预测治疗反应和自身免疫性疾病发生(如乙酰胆碱酯酶受体自身抗体)的生物标志物。
 沈建飞 副主任医师 台州医院 心胸外科690人已读
沈建飞 副主任医师 台州医院 心胸外科690人已读 - 学术前沿 前入路左侧隆突下淋巴结清扫安全可行原创
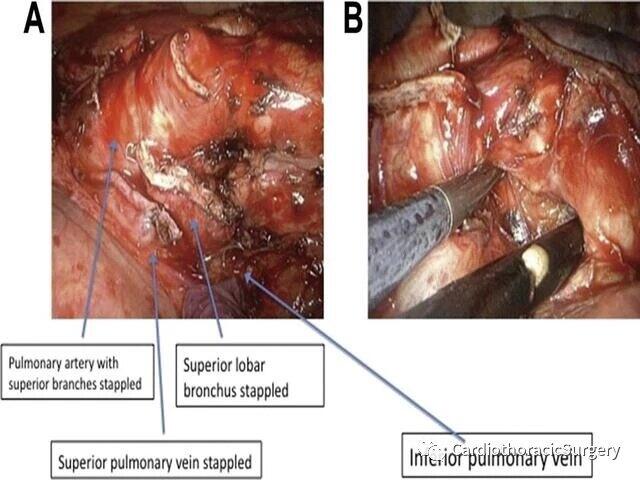
目前可手术切除的非小细胞肺癌(NSCLC)患者采取完整淋巴结清扫还是取样仍然存在争议。欧洲胸外科医师协会提倡完整解剖切除。然而,一些外科医生认为清扫,特别是左侧隆突下解剖切除是不恰当的。 鉴于此,来自法国的 Laura Haddad 医生等介绍了电视辅助胸腔镜手术(VATS)左肺叶切除术后,进行前入路隆突下淋巴结清扫术的手术方式,文章发表在的 ATS 杂志上。 手术过程:标准前入路 VATS 手术,依次解剖左上肺或左下肺血管、叶间裂和支气管,并予以离断,然后行完整的淋巴结清扫。采用前入路隆突下淋巴结清扫。 图 1. 术中图片 A: 从左向右英文标注依次为肺动脉-上肺动脉残端、上肺静脉残端、上肺支气管残端、下肺静脉; B: 隆突下使用吸引器轻轻地提起支气管。 使用无创钳牵引提气支气管残端,也可以提起主支气管而不挂持支气管(图 1),打开隆突下间隙,可以很容易地解剖和切除隆突下淋巴结(图 2)。为了显露的更好,可以在支气管隆突下使用吸引器轻轻地提起(图 1)。 图 2. 手术示意图,A: 红色圆圈为隆突下间隙;B: 打开隆突下间隙,解剖和切除隆突下淋巴结(箭头所示)。 隆突下淋巴结通常采用后入路清扫,因此需要牵拉剩余肺组织,术中暴露困难。该操作在下肺静脉后面执行,位于左主支气管内侧面,可能会损伤支气管微血管,常引起支气管坏死和支气管瘘。Laura Haddad 医生报道的前入路左侧隆突下淋巴结清扫可使隆突下淋巴结清扫简单、易行。
 沈建飞 副主任医师 台州医院 心胸外科1192人已读
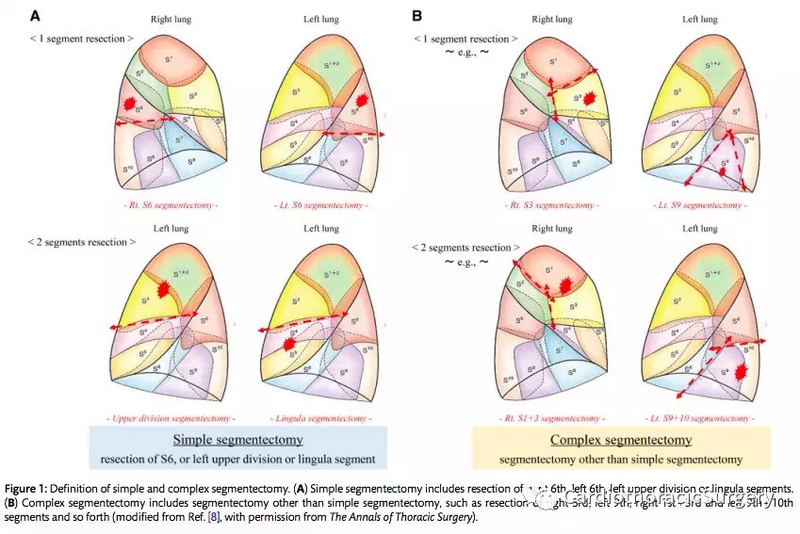
沈建飞 副主任医师 台州医院 心胸外科1192人已读 - 学术前沿 复杂肺段切除术治疗IA期非小细胞肺癌的长期结果
尽管针对早期肺癌的肺段切除术已广泛接受,但对于产生数个错综复杂段间平面的复杂肺段切除仍存在争议。潜在的争论包括无法治愈的风险和“肿瘤控制失败”。鉴于此,来自日本的Yoshinori Hand教授等开展了一项研究,比较了复杂肺段切除术与肺叶切除术治疗IA期NSCLC患者的结局,并评估其在肺癌治疗中的应用情况。研究结果发表在近期的EJCTS杂志上。 研究者回顾性分析了2009年4月至2017年12月间接受复杂肺段切除术(n=99)或肺叶切除术(n=94)的临床IA期肺癌患者资料。比较两组间的临床病理因素和术后结果。通过Kaplan-Meier方法和Cox回归分析评估影响预后的因素。 研究者发现两组间的30天死亡率(0% vs 0%),总体并发症发生率(26.3% vs 21.3%)和长时间漏气率(11.1% vs 9.6%)均未发现显著差异。复杂肺段切除术或肺叶切除术的5年总生存率(分别为93.5% vs 96.4%; p=0.21)或无复发生存率(分别为 92.3% vs 88.5%; p=0.82)两组无显著差异。复杂肺段切除术后复发2例(2.0%),肺叶切除术后复发7例(7.5%)(p=0.094),两组切缘复发率为0(0%)。多变量Cox回归分析显示,复杂的肺段切除术和肺叶切除术对无复发生存率的影响在数值上相似(危险比0.93,95%置信区间0.32-2.69;p=0.90)。 所以研究者认为,复杂的肺段切除术在早期肺癌治疗中提供了可接受的短期和长期结果。在这项回顾性研究中,复杂肺段切除术在短期和长期生存结果与肺叶切除相似。 将来有必要进一步研究复杂肺段切除术治疗肺癌。 原文题目:Complex segmentectomy in the treatment of stage IA non-small-cell lung cancer
 沈建飞 副主任医师 台州医院 心胸外科563人已读
沈建飞 副主任医师 台州医院 心胸外科563人已读 - 就诊指南 病理低侵袭性肺腺癌的新放射学标准
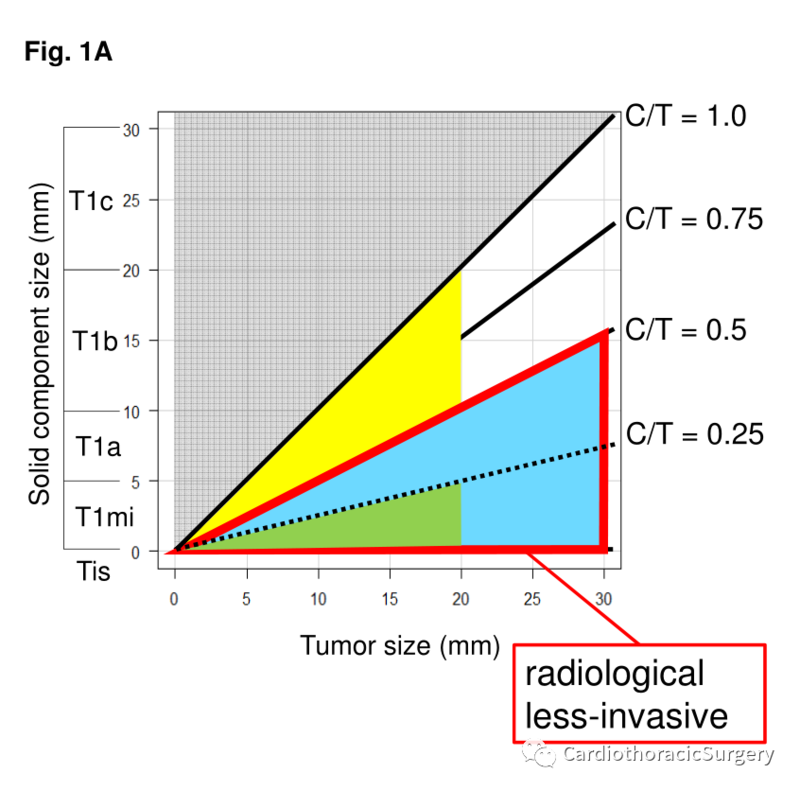
摘要 目的:日本临床肿瘤学组研究0201提出了薄层计算机断层扫描(TSCT)的放射学标准,以助于诊断病理低侵袭性肺腺癌,基于先前TNM分期这部分患者可能是亚肺叶切除的候选者(肿瘤≤3cm,C/T比≤0.5,无淋巴结和脉管浸润)。本研究的目的是根据第8版TNM分期,提出新的放射学标准来预测病理低侵袭性肺癌。 材料和方法:我们纳入2003年至2011年间744例周围型临床Tis-T1cN0M0期,且肿瘤≤3cm,接受根治性肺叶切除的非小细胞肺癌患者资料。将低侵袭性肺癌标准定为无淋巴结转移,无血管侵犯的肺癌,根据实性成分大小,实性/肿瘤(C/T)比(使用最大实性成分直径除以最大肿瘤直径计算放射学标准),通过使用术前TSCT预测特异性定为≥97%,并评估总存活率。 结果:研究者发现,除了1例患者,所有临床Tis / T1mi / T1a患者均为病理低侵袭性肺癌(特异性:99%)。从C/T比的研究来看,只有C/T比≤0.5的患者符合标准(特异性:100%)。结合这些标准后的最终特异性为99.6%,且显示出良好的预后(5年总生存率:96.2%)。 结论:临床表现为Tis/T1mi/T1a或C/T值在0.5以下的肺癌,因其病理上侵袭性较小,在保证足够切缘的情况下行亚肺叶切除术可以达到完全治愈。 前言 自1960年以来,可手术切除肺癌的标准手术方式仍然是肺叶切除术。唯一比较肺叶切除术和亚肺叶切除术的随机对照试验表明,即使在IA期非小细胞肺癌(NSCLC)患者中也不应使用亚肺叶切除术。然而,随着诸如薄层计算机断层扫描(TSCT)或正电子发射断层扫描(PET)的放射学诊断方式的迅速发展,近年来早期肺癌的诊断率一直在增加。日本临床肿瘤学组(JCOG)的肺癌外科研究组(LCSSG)进行了一项前瞻性研究,提出了放射学标准,可预测无淋巴结转移或血管浸润的病理性侵袭性较小的肺腺癌(JCOG 0201试验),他们将放射学低侵袭性肺肿瘤定义为C / T比为0.25或以下的2 cm或以下的肺肿瘤。随后,Asamura等人报道,C/T比值小于或等于0.5的3 cm以下肺癌预后极好。由于这些肿瘤可能是亚肺叶切除、肺段切除或宽楔形切除的主要候选者,两个针对这些肿瘤的前瞻性试验和另一个与亚肺叶切除有关的前瞻性试验已经在日本进行 (JCOG 0804、1211和0802试验)(图1A)。但是,TNM分类在2016年进行了大幅度修改,除了GGO成分外,实性成分的大小被重新采用作为对T分类进行分类的重要参数。在这项研究中,我们重新考虑了根据实性成分大小预测病理低侵袭性肺癌的最佳放射学标准。本研究的目的是提出新的放射学标准,通过考虑实体成分的大小来预测病理低侵袭性的肺癌(无淋巴结转移或血管侵犯),并将其应用于亚肺叶切除。 材料和方法 患者 我们回顾性评估了2003年1月至2011年12月在我院接受肺叶切除术或者更大范围切除实现了完全R0切除的临床肿瘤大小为3.0 cm或更小的Tis-T1cN0M0 NSCLC的患者。肿瘤中心位于TSCT上肺野外1/3的被定义为周围型肿瘤。接受术前治疗的患者或资料不足的患者被排除在该队列之外。在这项研究中,我们总共对744名患者的结果进行了统计分析。 这项回顾性研究是在国家癌症中心东部机构审查委员会(No.2016-399)的批准授权下进行的。 放射学评估 我们通常在手术前60天内进行TSCT。两名作者(S.K.和K.A.)回顾了手术前的TSCT图像,以评估肿瘤大小,实性成分大小,GGO成分,C / T比值以及其他特征。实性/肿瘤(C/T)比通过最大实性成分直径除以最大肿瘤直径计算(图1B、1C)。在带有肺窗,-600 HU的窗高度和1800 HU的窗宽度的监视器显示器上评估这些特征。观察员之间的测量误差以协商一致的方式得到纠正。在TSCT上,GGO区域被定义为在不遮挡基础血管结构的情况下增加的模糊密度区域,相反,实心区域被定义为完全遮盖基础血管结构的密度增加的区域。C/T比值定义为TSCT上实体成分最大尺寸与肿瘤最大尺寸的比值。临床淋巴结分期通过对比CT和/或PET来确定。纵隔淋巴结在TSCT上最短尺寸大于1.0厘米,和/或显示异常摄取18F-氟-2-脱氧-D-葡萄糖(FDG),被定义为淋巴结阳性肿瘤。必要时,进行经支气管内超声引导的经支气管针吸细胞学(EBUS-TBNA)检查,用于临床分期。然后根据第8版TNM分类进行肿瘤分期。 病理评估 所有切除标本均用10%福尔马林固定,石蜡包埋。连续4?m切片,苏木精-伊红(HE)染色。血管或淋巴管的浸润和胸膜浸润可通过HE和Victoria blue–van Gieson染色进行鉴定,以可视化弹性纤维。根据2015年世界卫生组织关于肺、胸膜、胸腺和心脏肿瘤的分类,S.K.和G.I.对组织类型和病理肿瘤大小以及侵袭性成分的大小进行了审查。肿瘤的分期基于国际肺癌研究协会第八版的TNM分类。 与放射学评估相关的敏感性和特异性可预测病理性浸润性肺癌 表1显示了与放射学评估相关的敏感性和特异性表,以预测病理性浸润性肺癌。表1中C组的患者在放射学上表现为侵袭性较小的肿瘤,但在病理学上显示为浸润性癌。对这部分患者进行亚肺叶切除被认为是一种治疗不足,导致局部复发率增加,或预后不良。需要减少C组的患者,以避免治疗不足,因此由D/(C+D)计算的特异度必须为越高越好。因此,我们把保持高度特异性作为首要目标。另一方面,B组中放射学上为侵袭性癌症但病理上侵袭性较小的癌症的患者数量也应该减少到最低。因为他们冒着过度治疗的风险,有可能失去接受亚肺叶切除的机会,这是一种保留功能的手术。但是,过度治疗可能不会导致严重的后果,因此我们决定将保持较高的灵敏度作为次要对象。在先前的研究3之后,我们将特异性标准设定为97%或更高,以最大程度地减少因亚肺叶切除而未得到治疗的肿瘤的数量,并研究了新的放射学标准,该标准可以满足最高敏感性的标准。 生存分析 所有患者术后随访至少5年,最长随访10年。在患者不能定期就诊的情况下,尽可能多地通过随访数据获取生存信息,随访时间长达10年。总生存时间(OS)被定义为从手术日期到最后一次随访日期或因任何原因死亡之间的时期。在患者还活着或失去随访的最后一次随访中对观察结果进行检查。我们机构的数据截止日期为2016年5月。 单因素分析采用Kaplan-Meier法,生存差异采用对数秩检验。双侧P值小于0.05的被认为具有统计学意义。所有数据均使用EZR 1.32版进行分析。 结果 病人特征 中位随访期为80个月(范围0.6~150.6)。表2显示了患者的临床病理特征。约55%的患者是男性,40%的患者从未吸烟。约40%的患者为GGO,所有患者病理上均为腺癌。病理淋巴结转移80例(11%),淋巴浸润78例(10%),血管侵犯197例(26%)。290例患者进行表皮生长因子受体(EGFR)突变检测,其中113例EGFR突变阳性。 病理浸润性或微侵袭性肿瘤的放射学特征 图2显示了所有744个肿瘤的放射学特征,根据术前放射学发现。黑点表示病理浸润性肿瘤(239例)。中空点代表病理低侵袭性肿瘤(505例)。根据放射学发现,肿瘤在地图上被标记在适当的位置。病理性侵袭性肿瘤多呈C/T比值1.0的直线分布。临床T1a(cT1a)或以下类别中也有一些病理浸润性肿瘤。 实性成分大小预测病理低侵袭性肿瘤 我们调查了三种基于实性成分大小的放射学标准。这些实性成分尺寸标准包括10mm或更小(等于cT1a或更小),15mm或更小和20mm或更小(等于cT1b或更小)。表3A显示了符合这些标准的结果。以实体成分小于或等于10 mm为标准,仅1个肿瘤为病理性侵袭,其特异性和敏感性分别为99.6%(238/239,95%CI:97.7~100.0%)和29.3%(148/505, 95%CI:25.4~33.5%)。小于或等于15mm的特异性84.5%(202/239,95%CI:79.3~88.9%),小于20mm的特异性为54.4%(109/239,95%CI:47.8~60.8%)。只有实性成分小于或等于10 mm(相当于临床T1a或更小)标准的特异性达到预先指定的阈值97%或更高。 C / T比或GGO成分预测病理性低侵袭性肿瘤 我们根据C/T比和GGO成分对三种放射学标准进行了研究。这些标准包括C/T值小于或等于0.5,小于或等于0.75,以及含有GGO成分的肿瘤。结果总结在表3B中。对于C / T比为0.5或更低的标准,特异性和敏感性分别为100.0%(239/239,95%CI:97.7–100.0%)和25.7%(130/505,95%CI:22.0–29.8%)。当C/T≤0.75时,特异度和敏感度分别为96.2%(230/239,95%CI:93.0~98.3%)和40.2%(203/505,95%CI:35.9~44.6%)。以GGO为标准,特异性为91.2%(218/239,212,95%CI:86.9~94.5%)。结果,只有C/T比为0.5或更低的标准超过预先规定的阈值。 新放射学标准对生存结果的影响 我们调查了放射学和病理学结果的相关性,并检测到符合预先指定阈值的新标准。这些肿瘤是cT1a或更小,C/T比等于或小于0.5,符合这些标准的肿瘤在本研究中被认为是侵袭性较小的肿瘤 (图3A)。综合这些标准,最终的特异度和敏感度分别为99.6% (238/239,95%CI:97.7~100.0%)和30.7%(155/505,95%CI:2 6.7~34.9%)。最后,我们调查了新标准的预后价值。图3B显示了放射学低侵袭性肿瘤和侵袭性肿瘤的总存活率的比较。放射学低侵袭性肿瘤的总存活率明显好于侵袭性肿瘤(p0.5的cT1b肿瘤中有病理浸润性肿瘤。由于这些肿瘤的侵袭性,我们在进行亚肺叶切除时必须小心,但总肿瘤直径在2 cm以下的肿瘤的预后良好,因此我们应该在前瞻性研究中评估这一点。这些肿瘤被纳入日本正在进行的关于节段性切除术的非劣效性的JCOG 0802试验中,并被纳入一项随机对照试验中,该实验旨在比较亚肺叶切除(节段切除或楔形切除)和肺叶切除术(CALGB-140503,NCT) -00499330;ClinicalTrials.gov),这些结果尚未公布。 这项研究有几个局限性。首先,这是对单个机构数据库的回顾性研究。其次,TSCT中实性成分的精确测量在世界范围内存在争议,因为观察者对GGO成分的评估往往不同。鉴于此,据报道,观察者之间很难就腺癌的亚类达成一致。为了将影响降到最低,我们评估了所有患者的术前TSCT图像;这些图像由两位观察者独立评审,然后观察者之间测量结果的差异被一致纠正。但是,我们没有评估观察者之间的一致性比率,因此,提高观察者的一致性是未来调查的一个挑战。第三,我们调查了一小部分纯实体的亚厘米肿瘤,所以即使是cT1a状态,纯实体肿瘤的侵袭性大小也是不清楚的。Sakurai等人报道说,没有GGO成分的亚厘米级肿瘤的病理性淋巴结受累率为10%。Hattori et等人报道PET的最大标准摄取值(SUVmax)对亚厘米非小细胞肺癌的预后有影响,特别是在纯实体肿瘤中。将SUVmax纳入术前标准可能有助于更准确地预测侵袭性较小的肿瘤。 结论 我们确定了放射学低侵袭性癌症患者的新标准,这些患者可能是合适的亚肺叶切除候选患者。cT1a或以下、C/T比值小于或等于0.5的肿瘤,放射学上侵袭性较小,预后良好。需要进一步的前瞻性研究来证实这一假设。 临床实践要点 随着放射学诊断手段的迅速发展,近年来早期肺癌的数量一直在增加。对于周围型早期非小细胞肺癌,亚肺叶切除是一种保留功能的手术方式。JCOG0201在第7版TNM分类的基础上,提出了TSCT诊断病理性微浸润腺癌的放射学标准,但TNM分类目前修订为第8版,并新采用实体成分大小作为T分类的重要参数。而且许多位于外围的早期非小细胞肺癌在手术前不能进行组织学检查。选择亚肺叶切除的最佳放射学标准仍不清楚。回顾性分析744例3cm或更小的周围型临床Tis-T1cN0M0 NSCLC患者,研究表明,临床T1a或更小且C / T比0.5或更小的肿瘤可以预测病理性微浸润(无淋巴结转移和无脉管侵入)肺癌(特异性:30.7%)。并且预后良好 (5年总生存率96.2%)。据我们所知,这是第一个通过考虑实性成分大小来提出术前放射学标准来预测病理低侵袭性肺癌的研究。TSCT术前实性成分大小和C/T比值对预测肺癌的侵袭性有很大的潜力,有助于外科医生计划对低侵袭性肿瘤施行亚肺叶切除,效果良好。
 沈建飞 副主任医师 台州医院 心胸外科838人已读
沈建飞 副主任医师 台州医院 心胸外科838人已读 - 引用 肺转移瘤的治疗进展临床综述
2014-05-22 00:12 来源:丁香园 作者:沈建飞 字体大小 - | + 肺转移瘤切除是胸外科的常规手术,它作为晚期癌症患者个体化治疗一部分的趋势正逐渐递增。由于缺乏随机对照试验(RCT),转移瘤切除的疗效只能基于注册数据和术后的随访研究。这些回顾性研究主要纳入一个或少数几个转移灶,且一期手术与转移灶切除的间隔时间超过2-3年。据报道,5年存活率为30-50% ,然而这些研究病例的选择大多有预后良好的特征,所以肺转移瘤与生存率之间的表观关系不能解释为因果关系。来自英国伦敦大学的Tom Treasure教授等人根据病理结果,将肺转移瘤分为四组进行证实。作者认为非精原细胞瘤,对化疗高度敏感,切除残存的肺部转移灶对后续治疗具有指导意义,尤其是对进一步化疗有着明确意义。肉瘤转移的靶器官主要是肺,骨和软组织肉瘤肺转移灶的切除是常规治疗选择,但并无随机临床试验数据支持。结直肠癌肺和肝转移最常见,反复切除和消融虽然司空见惯,但亦无可靠治疗依据。黑色素瘤预后极差,在无其他治疗方案可选时肺转移灶切除是可行的。本综述通过回顾现有证据并得出的结论,因缺乏随机临床试验数据而不能确定是否可靠。目的1、回顾支持肺转移瘤切除的证据并评估其可靠性2、就肺转移瘤切除的时间和部位达成某些共识3、探索以观察性研究作为可靠证据存在的潜在风险肺转移瘤的临床表现除了肺癌手术外,转移瘤切除是胸外科开展的最多的手术。在欧洲,转移灶切除达到了胸外科工作量的15-50%。大部分肺转移瘤患者曾接受过针对原发灶的治疗,通常于常规检查时(如全身CT平扫)发现。某些转移灶在胸科门诊查体或常规X片中发现,但转移灶的相关信息大多数仍来自肿瘤科医生。肺转移瘤的症状一般无特异性。转移瘤有时会侵犯胸壁引起胸痛,癌灶大量坏死时可引起反复咯血,抑或导致持续性肺炎,最终为了减轻症状而不得不选择手术切除。1997年国际肺转移瘤注册中心的数据肺是仅次于肝脏的另一个最常见转移部位。1997年,国际肺转移瘤注册中心(IRLM)报道来自欧洲和北美的5206例患者的文章具有里程碑意义。IRLM根据原发肿瘤的不同将分成4组:生殖细胞瘤(7%),黑色素瘤(6%),肉瘤(42%)和上皮瘤(44%)。注册中心和研究机构一致发现:不论何种肿瘤,原发灶切除术后转移瘤出现的时间间隔越长和转移灶越少,转移瘤术后患者的生存时间就越长。注册中心46%的患者为单个孤立转移灶,其中32%自原发肿瘤切除后的间隔达3年以上。这些特性可使患者的生存获益。18%的患者存在这两种特性,其中位生存时间为61个月,而没有这两种特性的患者中位生存时间为14个月。不同类型肿瘤的5年生存率大相径庭:非精原细胞瘤(NSGCT)为68%,上皮源性肿瘤37%,肉瘤为31%和黑色素瘤为21%。目前,结直肠癌(CRC)肺转移瘤是主张手术切除的最常见的上皮源性肿瘤。乳腺癌和肺癌的肺转移瘤则很少考虑手术。妇科、泌尿系和上消化道肿瘤常常同时出现。甲状腺和肾可能存在孤立和缓慢生长的转移灶,因病例数很少,所以不单独进行分析讨论。主要关注于应用证据的性质。寡转移1995年,有人提出寡转移的临床状态,认为可以采用治愈性治疗方案。寡转移指限于5个或更少的转移,也可能出现于多个器官。一篇该领域的综述表明,此结论既不是生物实体也并非基于转移频率分布的数学分析得出,而是转移灶≤5个时便于采用消融术进行治疗。肿瘤标志物在筛查中的作用人绒毛膜促性腺激素(hCG)和α-胎球蛋白常用于检测NSGCT的持续或复发。癌胚抗原(CEA)升高大于5μg / L对CRC诊断具有特异性,但也可能存在于间皮瘤和其他肿瘤。Dukes’A,B,C和D期升高率分别为3%、25%、45%和65%。CRC根治性切除后CEA会随之下降,随后再升高则与肿瘤转移密切相关,尤其是肝转移。CEA升高与CRC患者肺转移的不良预后相关,该指标可能是一把双刃剑:CEA升高可能预示着发生了肺转移,但又可引导下一步的抗转移瘤治疗。现已证实以CEA升高为指标的研究和外科手术均不能改善患者的生存率。目前临床中应用大量的肿瘤标记物检测,存在许多不合理,原因是其成本高,且可导致进一步进行无益的检查。非精原细胞瘤肺转移NSGCT最常见于年轻男性,对化疗高度敏感,其中90%能治愈。8%的I期患者会发生肺转移。IRLM数据显示2-3年后NSGCT的生存曲线出现一个显著的平台期,这与它的高治愈率相符。化疗后肺部可能存在残留肿块,可能是坏死组织或恶性肿瘤残留。1/3的病例是恶性肿瘤,其组织学类型与原发癌不同;因此,NSGCT手术切除有效,且有助于指导进一步的治疗和化疗。欧洲学会胸外科医师(ESTS)肺转移瘤项目将NSGCT肺转移瘤作为其评估的一个部分。检索从1998年至2009年,将病例数≥50且手术时间不早于1980年的文献进行分析。共纳入六项研究包括740例患者,平均年龄为27岁。已报道的肺转移后5年生存率为73%-94%。多发转移和恶性肿瘤残留与疾病进展和死亡相关。研究发现,非活动性病灶存在坏死的病人应避免化疗。如果一侧肺转移瘤出现坏死,95%的病例对侧肺存在相同的坏死。这可能表明对侧肺可免做手术。远期生存率不仅仅归因于手术,然而令人信服的证据表明,手术是一个切实可行的治疗方案。目前NSGCT肺转移瘤切除患者的适应症包括:1.对化疗不敏感;2.复发病灶对化疗有部分反应;3.标准和二线化疗后复发;4.确定是否存在残余有活性的肿瘤;5. 切除肿瘤增大的良性畸胎瘤成分。肉瘤肺转移一项系统性回顾分析报道了15例接受初始肺转移瘤切除术治疗的患者:骨肉瘤5例,软组织肉瘤6例和混合瘤4例。肉瘤包括多种病理实体,但在已发表的一系列肺转移瘤切除文献中其描述的处理方式没有明确区别,本综述范围有限将其一起考虑。肉瘤转移可能局限于肺,转移灶切除是处理肉瘤的一种有效方法。骨肉瘤研究协作组发现,诊断为存在转移瘤的202例患者中81%有肺转移,以及62%只有肺转移。一项三个欧洲骨肉瘤研究机构(EOI)关于化疗的RCT分析表明,564例患者出现复发,其中307(54%)例只有肺转移。2006年, 英国国家临床规范研究院(NICE)在英格兰和威尔士发行了国家健康服务指南,为癌症服务委员出版了一本‘改善肉瘤患者预后’的手册。该手册指出,需要更多组织参与而非单纯的指导临床实践,需要一个包括胸外科医生在内的肉瘤多学科团队。该系统回顾纳入18项随访研究,报道了从1991年到2010年出版文献中肺转移瘤切除的筛选标准和结果。1196例患者初始接受转移瘤切除术。1357例患者中43%随后接受转移瘤切除术,部分患者接受开胸术≥10次。三项研究局限于肺转移瘤复发患者。以5年生存率为观察指标。无RCTs或其他形式的比较分析。关于症状或生活质量的数据未见报道。骨和软组织肉瘤,首次转移瘤切除术后患者的5年存活率分别为34%和25%。系列研究报道了多因素分析结果:转移瘤的数量越少及明确诊断后出现转移瘤的时间间隔越长,患者的生存率更高。1995-2004年间泰晤士河癌症注册中心的所有骨肉瘤转移患者的5年生存率为25%,软组织肉瘤转移为15%。鉴于肺转移瘤切除术常用于高选择性的少数患者中,这表明转移灶切除术的获益不能放大。尽管转移瘤切除是治疗肉瘤的一个‘标准’组分,但其临床获益的证据太少。黑色素瘤肺转移黑色素瘤肺转移瘤切除术作为ESTS肺转移瘤切除项目的一部分而进行评述。两个出版物包括注册数据。1971-1993的22年间约翰·韦恩癌症研究所(JWCI)有6129例,1970-2004的32年间杜克大学有14 057例。这些数据使我们得以从数字的角度看待黑色素瘤肺转移瘤切除术在美国的应用情况。至少存在一个肺转移瘤的发病率分别为16% (984/6129)和12%(1720/14 057)。存在肺转移的患者中行肺转移瘤切除分别为11%和18%,该差异可能反映了在后续的10年里增加了对肺转移瘤切除的兴趣。随后JWCI报道45例通过普通胸部X线平片计算肿瘤在体内的倍增时间,该研究显示倍增时间越短患者的预后越差,这也说明不考虑转移瘤切除的作用时,肿瘤的生物学特性是预后的重要决定性因素。免疫治疗可限制微小黑色素瘤,肉眼可见的残留肺转移灶行手术切除。ESTS综述作者建议应严格限制黑色素瘤肺转移手术切除的指证。ESTS专家认为,仅仅凭这些证据还不能给出合理建议。结直肠癌肺转移过去50年,大约有100篇关于CRC转移瘤的报道,但无随机对照研究。目前信息最全面的是由西班牙注册中心最近发表的一篇543例报道。2008年3月至2010年2月,由西班牙GECMP-CCR成立的国家注册中心,收集了来自32个胸外科单位手术切除单个或多个结节,且组织学证实为肺转移瘤的所有患者数据。男性占65%,年龄32 - 88(平均65)岁。55%的患者为单个孤立转移灶。原发灶切除和出现转移瘤的时间间隔中位数为28个月,且大部分患者CEA水平偏低或正常。29%的患者出现肺转移瘤前已存在肝转移。自十九世纪60年代中期,一篇全面的综述表明:随着时间的推移混合病例如何相对减少。平均年龄由60岁增加到65岁,单发转移瘤患者的比例从60%下降到55%。然而,先前存在肝转移病人的比例显著上升。最近一项系统评价和荟萃分析将CRC肺转移瘤切除结果考虑在内。该分析纳入了25篇研究,共2925例患者。完全切除肺转移瘤术后患者总的5年生存率为27%-68%。离群数往往是较小部分。三个预后因素与低生存率相关:(i)原发肿瘤切除和肺转移瘤出现的无病生存时间间隔短(HR 1.59,95%CI:1.27,1.98);(ii)多发转移瘤(HR 2.04,95%CI:1.72-2.41);(iii)开胸前CEA水平高(HR 1.91,95%CI:1.57-2.32)。肺门和/或纵隔淋巴结转移阳性(HR 1.65,95%CI:1.35-2.02),患者的预期结果较差,而与是否存在肝转移瘤切除史(HR 1.22,95%CI:0.91-1.64)并不重要。转移瘤切除术证据不足肺转移瘤切除证据绝大部分是基于随访研究,不可避免地存在严重偏倚。IRLM数据的局限性是缺乏标准。该缺陷是大部分外科术后随访的核心:只针对完成治疗患者的数据。最重要的局限是选择性偏倚。只有2-3%的患者出现肺转移瘤,也就是说,每30-50例患者只有1例进行了肺转移瘤切除术。选择手术切除患者具有良好的特性:单个或少数几个转移瘤,距原发灶术后手术间隔时间长,结直肠癌CEA未升高。无论患者是否接受治疗,这些普遍的预后特征与生存率相关。肺转移瘤切除报道的共同缺陷是难以区分预后和预测的特性。无论治疗与否,预后因素较好的患者可能存活的时间更长,预测性因素可判断患者能否从特定的治疗中获益。消极预测特征包括(i)不能控制的原发肿瘤,(ii)其他部位转移,(iii)不能达到显微镜下切缘阴性(R1/2),(iv)纵隔淋巴结转移。外科医生认为前两点应排除,他们会尽力避免第三和第四点,因为不能达到清除肿瘤的目的转移瘤切除术是失败的。最近很多研究在发表时排除了未能达到R0切除的患者。除了这些已知的预后和预测因素,医生和多学科团队在众多非特异的临床标准下筛选病人。在同一时间点获取和录入数据进行多元分析。临床医生视患者情形尝试进行两次,三次或者更多次手术。有经验的临床医生能辨别哪些患者的预后可能不是很好,他们知道如何去选择预后较好的患者。无痛性疾病已与临床恶化和影像学进展的侵袭性较强的恶性肿瘤进行了区分。这种高效的选择方式并未纳入数据库、注册中心或随访研究。临床医生发现在无明确对照组的情况下接受转移瘤切除术的患者相比IV期肿瘤患者预后较好。但接受转移瘤切除的患者通常在原发肿瘤切除时没有明显的转移灶,且平均在2-3年后才出现转移灶。这类患者不应只单纯与一开始就出现转移灶的患者比较,而应进一步与分期相似患者在临床表现或一期手术方面的生存率进行混合比较。通常认为所有存在转移瘤的患者都有短期的预后。30年前的一项小型研究报道了12例符合肺转移瘤切除标准但未接受转移瘤切除术的患者,资料来源于呼吸内科医生的临床病历。5年后12例患者中仍有3例存活 (25%;95% CI 5.49% to 57.19%)。berg指出“现有的假设、暗示或声明指出非手术患者的5年生存率为“0”。然而事实并非如此,肿瘤注册中心许多肉瘤和CRC转移瘤患者的情况也并非如此。通常提倡对化疗有反应或无进展的患者进行转移瘤切除或再次转移瘤切除。在这部分患者中无法区分特定干预措施的疗效,但在转移瘤切除组其生存获益似乎可以归因于手术。通常纳入手术的要求是化疗后无进展的患者。表面上患者为了生存接受转移瘤切除术,而不是转移瘤切除本身延长患者的生存时间。这是时间偏倚的一种永恒现象。通常认为第二次或第三次转移瘤切除可再次控制或“重置肿瘤时钟”,却忽视了正在降低转移瘤切除的标准。二期或三期治疗后仍然存活的患者才有资格纳入综合治疗组,而不是以存活作为治疗的结果。结论尽管有很多回顾性研究,但是肺转移瘤切除术的证据仍不充分。目前还没有RCT,且缺乏比较性分析。该手术感觉以需要“做些什么”才得以开展,最明显的是患肉瘤的年轻患者反复进行肺切除术。肺转移瘤切除和生存率之间可能存在关系,但它并未通过布拉德福德-希尔的因果关系测试(Bradford Hill tests)。考虑到疾病的异质性,进展性以及治疗的多样性和重复性,要想从混杂信息中识别出有用信息是较困难的。肺转移瘤切除术的疗效仍不明确,除非有充分的RCTs证据证实。迄今为止,最常见的转移瘤切除指征是CRC,因此PulMiCC试验仅限于该病且正在招募中。
秦建军 主任医师 医科院肿瘤医院 胸外科2635人已读





